Περιεχόμενο
Τα πρωτόνια, τα νετρόνια και τα ηλεκτρόνια είναι τα τρία κύρια σωματίδια που σχηματίζουν ένα άτομο. Όπως υποδηλώνουν τα ονόματά τους, οι πρώτοι χρεώνονται θετικά, οι τελευταίοι δεν έχουν καμία χρέωση (είναι ουδέτεροι) και ο τρίτος έχει αρνητική χρέωση. Τα ηλεκτρόνια έχουν πολύ μικρή μάζα, ενώ τα πρωτόνια και τα νετρόνια έχουν σχεδόν ίδια μάζα. Μπορείτε να βρείτε τον αριθμό καθενός από αυτά σε ένα άτομο χρησιμοποιώντας μόνο πληροφορίες από τον περιοδικό πίνακα.
Βήματα
Μέρος 1 από 2: Υπολογισμός πρωτονίων, ηλεκτρονίων και νετρονίων
Αποκτήστε ένα περιοδικό τραπέζι. Είναι μια εικόνα που οργανώνει τα στοιχεία με ατομική δομή. Κατατάσσεται ανά χρώμα και δίνει σε κάθε στοιχείο μια μοναδική συντομογραφία ενός, δύο ή τριών γραμμάτων. Άλλες πληροφορίες περιλαμβάνουν ατομική μάζα και αριθμό.
- Μπορείτε να βρείτε έναν περιοδικό πίνακα online ή σε ένα βιβλίο χημείας.
Βρείτε το στοιχείο σας στον περιοδικό πίνακα. Οργανώνει τα στοιχεία με ατομικό αριθμό και τα χωρίζει σε τρεις κύριες ομάδες: μέταλλα, μη μέταλλα και μεταλλοειδή (ημι μέταλλα). Άλλες ομάδες περιλαμβάνουν αλκαλικά μέταλλα, αλογόνα και ευγενή αέρια.- Η χρήση της ομάδας (των στηλών) ή της τελείας (οι σειρές) μπορεί να κάνει το στοιχείο πιο εύκολο να βρεθεί στον πίνακα.
- Μπορείτε επίσης να αναζητήσετε το σύμβολο του στοιχείου εάν δεν γνωρίζετε άλλες ιδιότητες.
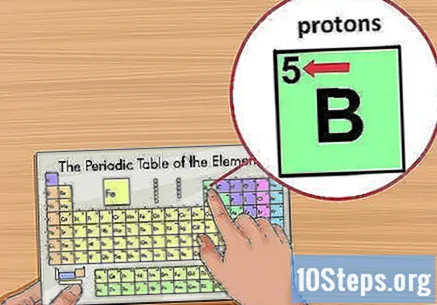
Εντοπίστε τον ατομικό αριθμό. Βρίσκεται πάνω από το σύμβολο του στοιχείου, στην επάνω αριστερή γωνία του τετραγώνου. Ο ατομικός αριθμός θα σας πει πόσα πρωτόνια σχηματίζουν ένα άτομο αυτού του στοιχείου.- Για παράδειγμα, το βόριο (Β) έχει ατομικό αριθμό 5 και συνεπώς πέντε πρωτόνια.
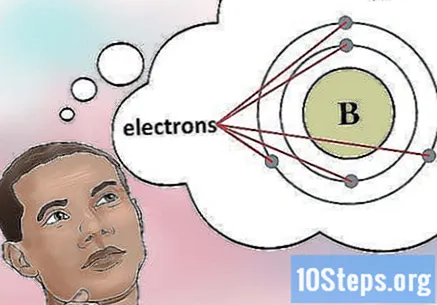
Προσδιορίστε τον αριθμό των ηλεκτρονίων. Τα πρωτόνια είναι σωματίδια στον πυρήνα ενός ατόμου που έχουν θετικό φορτίο. Τα ηλεκτρόνια είναι αρνητικά φορτισμένα σωματίδια. Επομένως, ένα ουδέτερο στοιχείο θα έχει τον ίδιο αριθμό πρωτονίων και ηλεκτρονίων.- Για παράδειγμα, το βόριο (Β) έχει ατομικό αριθμό 5 και συνεπώς πέντε πρωτόνια και πέντε ηλεκτρόνια.
- Ωστόσο, εάν το στοιχείο περιλαμβάνει θετικό ή αρνητικό ιόν, τα πρωτόνια και τα ηλεκτρόνια δεν θα είναι τα ίδια. Θα πρέπει να τα υπολογίσετε. Ο αριθμός ιόντων θα εμφανίζεται ως ένα μικρό υπεργράφημα μετά το στοιχείο.
Ψάξτε για την ατομική μάζα. Για να βρείτε τον αριθμό των νετρονίων, θα πρέπει πρώτα να βρείτε την ατομική μάζα. Αυτή η τιμή είναι η μέση μάζα των ατόμων ενός στοιχείου και βρίσκεται κάτω από το σύμβολο του στοιχείου.
- Στρογγυλοποιήστε την ατομική μάζα στον επόμενο ακέραιο αριθμό. Για παράδειγμα, η ατομική μάζα του Boron είναι 10,811, αλλά μπορείτε να την στρογγυλοποιήσετε έως το 11.
Αφαιρέστε τον ατομικό αριθμό από την ατομική μάζα. Για να βρείτε τον αριθμό των νετρονίων, πρέπει να αφαιρέσετε τον ατομικό αριθμό από τη μάζα. Να θυμάστε ότι ο ατομικός αριθμός είναι ίσος με τον αριθμό των πρωτονίων, που έχει ήδη αναγνωριστεί.
- Για το παράδειγμα Boron, 11 (ατομική μάζα) - 5 (ατομικός αριθμός) = 6 νετρόνια
Μέρος 2 από 2: Υπολογισμός ηλεκτρονίων με ιόντα
Προσδιορίστε τον αριθμό των ιόντων. Θα εμφανίζεται ως μια μικρή τιμή υπεργράφου μετά το στοιχείο. Ένα ιόν είναι ένα άτομο με θετικό ή αρνητικό φορτίο λόγω της προσθήκης ή της αφαίρεσης ηλεκτρονίων. Σε ένα ιόν, αν και ο αριθμός των πρωτονίων παραμένει ο ίδιος, αλλάζει ο αριθμός των ηλεκτρονίων.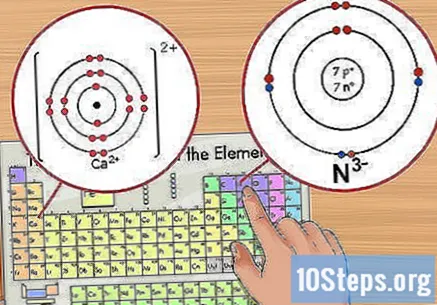
- Δεδομένου ότι το ηλεκτρόνιο έχει αρνητικό φορτίο, όταν αφαιρείται, το ιόν γίνεται θετικό. Καθώς προστίθενται περισσότερα ηλεκτρόνια, το ιόν γίνεται αρνητικό.
- Για παράδειγμα, το Ν έχει φόρτιση -3, ενώ το Ca έχει φόρτιση +2.
- Να θυμάστε ότι δεν χρειάζεται να κάνετε αυτόν τον υπολογισμό εάν δεν υπάρχει αριθμός υπεργράφου μετά το στοιχείο.
Αφαιρέστε το φορτίο από τον ατομικό αριθμό. Όταν ένα ιόν έχει θετικό φορτίο, το άτομο έχει χάσει ηλεκτρόνια. Για να υπολογίσετε το υπόλοιπο ποσό, αφαιρέστε το ποσό της επιπλέον χρέωσης από τον ατομικό αριθμό. Στην περίπτωση θετικού ιόντος, υπάρχουν περισσότερα πρωτόνια από τα ηλεκτρόνια.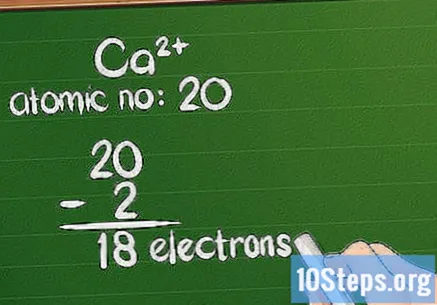
- Για παράδειγμα, το Ca έχει φορτίο +2, οπότε έχει χάσει 2 ηλεκτρόνια από τη φυσική του κατάσταση. Ο ατομικός αριθμός ασβεστίου είναι 20, έτσι το ιόν έχει 18 ηλεκτρόνια.
Προσθέστε το φορτίο στον ατομικό αριθμό για αρνητικά ιόντα. Όταν ένα ιόν έχει αρνητικό φορτίο, το άτομο έχει αποκτήσει ηλεκτρόνια. Για να υπολογίσετε τον συνολικό αριθμό αυτών, απλώς προσθέστε το ποσό της πρόσθετης χρέωσης στον ατομικό αριθμό. Στην περίπτωση αρνητικού ιόντος, υπάρχουν λιγότερα πρωτόνια από τα ηλεκτρόνια.
- Για παράδειγμα, το Ν έχει φορτίο -3, οπότε κέρδισε τρία ηλεκτρόνια σε σύγκριση με την ουδέτερη του κατάσταση. Ο ατομικός αριθμός αζώτου είναι 7, άρα αυτό το ιόν έχει 10 ηλεκτρόνια.